【2026 最新法規】化妝品PIF沒過關恐罰百萬?品牌上市前必看的法規地雷與省時清單

【文章摘要】
- 全面倒數:2026年7月1日起,沒備齊 PIF 檔案的化妝品將不得販售。
- 代價慘重:違者最高處 100 萬元罰鍰,但對品牌更致命的是強制下架與停業處分。
- 責任歸屬:法律規定「品牌商」才是第一責任人,受罰的是你!
- 5 分鐘讀懂 PIF:它不只是幾張紙,而是產品合法的身分證,更是品牌最強的風險防火牆。
- 16 項省時清單:快速拆解四大核心模組,教你如何有效對接代工廠與實驗室。
【文章目錄】
- 為什麼 2026 是關鍵期限?PIF 實施時程表
- 什麼是化妝品產品資訊檔案PIF?
- 誰負責 PIF 的準備?品牌商不可不知的法律責任
- 化妝品 PIF 必備清單,品牌商的省時對照表
- 如何高效準備化妝品產品資訊檔案 PIF?
- 最高罰百萬!PIF 沒過關後果這麼嚴重?
- 常見問答(FAQ)
- 結語
這幾年我們在代工第一線觀察到,化妝品市場已經悄悄變天。以前大家只要煩惱產品好不好用、包裝夠不夠美、行銷怎麼做會爆;但現在,品牌想活得長久合法才是重點。特別是 2026 年 7 月 1 日 這個大限,對很多品牌來說就像是一道檻。如果拿不出完整的 PIF(產品資訊檔案),再紅的明星商品也可能在一夜之間面臨百萬罰單,甚至被要求強制下架。
為了不讓大家辛苦建立的心血卡在法規這一關,創馳生技特別整理了這份實戰攻略。與其等到被抽查才焦頭爛額,不如現在就先弄懂規則,把風險降到最低。這篇文章會帶你一次看懂時間點、該備齊哪些文件,以及如何確保你的品牌能在這波新制中穩穩過關。
為什麼 2026 是關鍵期限?PIF 實施時程表
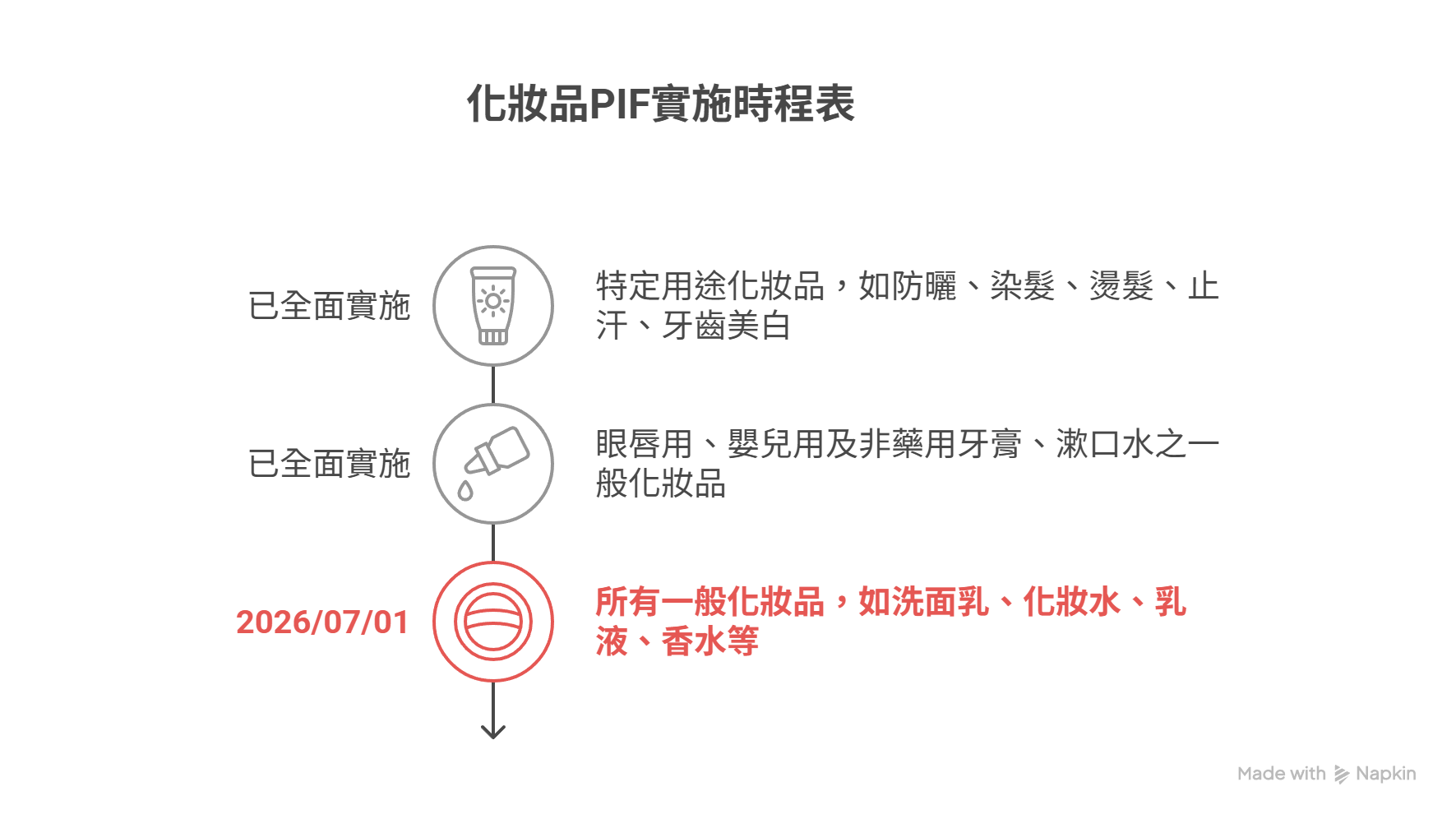
根據衛福部《化妝品衛生安全管理法》,所有化妝品都需要 PIF 文件才可以合法上市。很多品牌商會問:「PIF 不是講很久了嗎?為什麼大家最近才在緊張?」其實法規並不是一次性全面強制執行,而是採取三階段逐步推動。大多數品牌經營的保養品與香氛都落在第三階段。雖然看似還有時間,但PIF裡面的「安定性試驗」與「防腐效能挑戰」通常需要 3 到 6 個月的測試週期。建議提早做準備,避免錯過 7 月 1 日的合法上市期限。
| 階段 | 上路時間 | 適用產品類別 |
| 第一階段 | 已全面實施 | 特定用途化妝品(如防曬、染髮、燙髮、止汗、牙齒美白) |
| 第二階段 | 已全面實施 | 眼唇用、嬰兒用及非藥用牙膏、漱口水之一般化妝品 |
| 第三階段 | 2026/07/01 | 所有一般化妝品(如洗面乳、化妝水、乳液、香水等) |
什麼是化妝品產品資訊檔案PIF?
化妝品產品資訊檔案(Product Information File, PIF)就是化妝品的合法身分證。它是品牌商用來證明產品安全、合法且具備上市資格的完整技術文件。依據法規,化妝品在正式販售、贈送甚至提供試用前,品牌商都必須準備好這份檔案。掌握 PIF 的三大關鍵點
首先要提醒大家,根據衛福部《化妝品產品資訊檔案管理辦法》規定,PIF 必須以中文或英文來建立。除了語言要對,品牌商在實務管理這份產品身分證時,一定要抓穩這三個細節:- 不需主動繳交,但要隨時備查:PIF 不是送審文件,不需要事前寄給衛福部。它是存放在你公司內部的,但主管機關登門查核,品牌商必須能即時提出。
- 存放地點有規定:檔案不管是印成紙本還是存電子檔,都必須保存在品牌商的公司登記地址,不可以隨便放置在其他地方。
- 下架後仍要保留 5 年:這點最容易被忽略!就算產品已經停產、下架,該份 PIF 檔案還是得保存至少五年,以應對後續可能的追溯調查。
誰負責 PIF 的準備?品牌商不可不知的法律責任
很多老闆最常問的一句話就是:「東西是工廠做的,法規文件不是應該工廠負責嗎?」但這其實是最大的誤區。在法律眼裡,誰的名字出現在包裝上,誰就是 PIF 的第一責任人。雖然品牌商可以把整理文件這件事交給代工廠或專業顧問協助,但這份法律義務是轉嫁不掉的。如果把 PIF 比喻成產品的健保卡,代工廠就像是醫師負責提供檢查數據,但這張卡最後還是得由品牌商(持卡人)妥善保存。萬一遇到主管機關查核,品牌商必須能立刻拿出檔案。實務上我們會協助品牌商準備大部分的技術報告與數據,但檔案有沒有備齊、有沒有存放在公司、有沒有過期,這些法律責任最終都會回歸到品牌端。
| 類別 | 責任業者 | 說明 |
| 國產化妝品 | 製造業者(委託製造) | 若為OEM/ODM代工製造,責任仍由品牌商負責。代工廠通常可協助PIF建置。 |
| 製造業者(自產自營) | 由製造業者負責PIF建置。 | |
| 進口化妝品 | 輸入業者(代理/進口商) | 由負責進口與販售的業者負責PIF建置。 |
化妝品 PIF 必備清單,品牌商的省時對照表
很多人一聽到要準備 16 項文件就想退縮,其實只要釐清「誰手上有資料」,事情就簡單一半。我們幫大家整理了這張對照表,建議品牌商可以直接拿這張表去詢問代工廠,確認哪些部分工廠會幫你搞定。| 項目分類 | 16 項核心文件清單 | 資料從哪裡來? (建議來源) |
| 產品描述 | 01.產品基本資料 02.完成產品登錄之證明文件 03.全成分名稱及其各別含量 04.產品標籤、仿單、外包裝或容器 05.製造場所符合化粧品優良製造準則之證明文件或聲明書 06.製造方法、流程 07.使用方法、部位、用量、頻率及族群 08.產品使用不良反應資料 |
品牌商與代工廠 (多為產品開發時的基礎文件) |
| 品質資料 | 09.產品及各別成分之物理及化學特性 10.成分之毒理資料 11.產品安定性試驗報告 12.微生物檢測報告 13.防腐效能試驗報告 |
代工廠與原料商 (需實驗室數據支持) |
| 功能與包材 | 14.功能評估佐證資料 15.與產品接觸之包裝材質資料 |
檢測單位與包材供應商 |
| 安全評估 | 16.產品安全資料 | 專業安全資料簽署人員(SA) |
如何高效準備化妝品產品資訊檔案 PIF?
根據衛福部的《化粧品產品資訊檔案製作指引》,PIF 並沒有標準格式,它更像是一份證據清單。重點不在於文件準備得多厚,而是在於遇到查核時,這份檔案能不能做到「可追溯、可驗證」。高效準備 PIF 的秘訣
品牌商不需要自己變成法規專家。除了原物料商提供的規格書(COA)、學術文獻的安全性研究,最關鍵的夥伴就是你的代工廠。一個專業的代工夥伴,在生產研發時就應該幫你備妥製造流程、微生物檢測與安定性報告。化妝品 PIF 的 16 項核心內容:四大模組拆解
為了讓大家更有頭緒,創馳生技把這 16 項文件歸納成四個實戰模組,讓你一眼看懂準備方向:- 第一類:產品的身家調查(項目 01 - 08)
- 第二類:品質與實驗數據(項目 09 - 13)
- 第三類:外貌與宣稱的底氣(項目 14 - 15)
- 第四類:終極把關者(項目 16)
最高罰百萬!PIF 沒過關後果這麼嚴重?
為什麼衛福部要抓這麼兇?其實就是為了「安全」這兩個字。很多品牌商以為 PIF 只是應付公事,隨便交個報告就好。但只要出事,這份檔案就是用來證明品牌已經盡到安全責任的關鍵證據。如果你拿不出 PIF 或資料不全,在主管機關眼裡,這就等於是「來路不明且有風險」的商品。只要被查核到以下三種狀況,就會直接踩到法律紅線:- 完全沒準備:產品還沒上市、送人或提供試用,檔案就得先備齊。沒做就是違規。
- 資料隨便填:為了趕上市而偽造數據、造假成分資料,這比沒做更嚴重。
- 限期未改:稽查後被要求補件或修正,卻沒有在期限內處理好。
衛福部 PIF 處分與法律後果清單
這張表不是要嚇唬大家,而是要提醒違規的成本遠比找專業團隊做 PIF 還要高得多。建議品牌商在開發階段就納入 PIF 規劃,別讓辛苦建立的產品毀在法規風險上。| 風險類別 | 具體代價與法律限制 | |
| 金錢罰鍰 | 罰金 | 處新臺幣 1 萬元以上 100 萬元以下罰鍰。 |
| 按次處罰 | 違規情節沒改好就繼續罰,罰到合格為止。 | |
| 市場禁令 | 禁止流通 | 違規產品不能賣、不能送、甚至試用都不行。 |
| 回收/銷毀 | 主管機關命業者限期回收,不配合者沒入銷毀。 | |
| 撤銷資格 | 情節重大者,撤銷或廢止化粧品產品登錄。 | |
| 經營危機 (情節重大者) |
勒令停業 | 停業 1 個月到 1 年,這對任何公司都是致命傷。 |
| 公司註銷 | 最重可能廢止公司或工廠登記,等於品牌宣告終結。 | |
| 禁辦條款 | 登錄被廢止後,一年內該產品禁辦,明星商品將徹底消失一年。 | |
▲ 創馳生技製表:衛福部產品資訊檔案PIF處分與法律後果清單
常見問答(FAQ)
Q:我們是委託代工廠製造的品牌商,也要做 PIF 嗎?
A:是的。根據法規定 PIF 的建檔義務原則上由產品登錄人(品牌商)負責。不過實務上,品牌可委由代工廠或第三方專業單位協助建立,以確保內容符合最新法規。
Q:PIF 需要保存多久?
A:自產品最後上市日之次日起,至少保存五年,以供主管機關查驗備查。
Q:PIF 需要每年更新嗎?
A:法規並未強制規定更新頻率,但若產品有任何變更(如配方、原料來源、標示內容或包裝)時,應即時更新 PIF,以維持資訊正確性。
Q:PIF 需要主動繳交政府單位審核嗎?
A:無需主動繳交。PIF 為品牌內部備查文件,但主管機關於抽查或接獲檢舉時可要求調閱,品牌須於限期內提供完整資料。
Q:若同一產品有50ml、100ml 兩種容量,需做兩份 PIF 嗎?
A:若產品的配方、用途與標示內容完全一致,僅包裝容量不同,可在一份 PIF 中註明多種容量與包裝樣式,無須分別建檔。但需清楚列出各版本資訊以備查驗。
創馳生技專業代工,一站搞定法規風險
老實說,在代工第一線這麼久,我們最常看到品牌商遇到的挫折,並不是產品開發不出來,而是萬事俱備後,卻卡在「法規」這臨門一腳。最嚴重的後果,就是產品都已經鋪貨到通路上,卻因為文件不齊被主管機關要求撤櫃下架,那種損失與壓力,真的不該由品牌商獨自承擔。
這就是為什麼在創馳生技,我們不把自己定位成單純的「代工廠」。我們習慣在產品開發的初期,就把 PIF 的邏輯帶進來。當我們在討論配方時,就已經同步在篩選原料、規劃後續的測試需求,並預判安全評估(SA)的過關率。我們想做的,是讓你的產品在進工廠生產前,就已經具備經得起查核的體質。把這些繁瑣、燒腦的法規整合交給創馳,你就能把省下的時間與精力,全力放在市場行銷與品牌經營上。
〈延伸閱讀:化妝品新創品牌指南,上市備查流程與法規分類重點總整理!〉
結語
最後,我們想說的是2026 不只是期限,更是品牌升級的機會。法規的變動,短期看來雖然繁瑣,但長期來看,這其實是在幫台灣化妝品市場做一次大掃除。未來,能留在市場上的品牌,絕對是那些不僅懂產品、懂行銷,更懂得對消費者安全負責的專業經營者。
這幾年我們接觸過許多充滿熱情的創辦人,大家最擔心的往往不是產品不夠好,而是被這些生澀、甚至有點冷冰冰的法規條文擋住了去路。我們想告訴你的是你並不孤單,這些路我們已經幫客戶走過很多遍。與其讓自己陷在百萬罰鍰的擔憂中,不如把這些專業庶務交給創馳生技,讓你把最珍貴的時間,留給品牌最核心的行銷與通路拓展。2026 年 7 月 1 日很快就會到來,讓創馳生技成為你品牌上市最堅強的後盾,歡迎隨時與我們聯繫。

〈產品介紹:香氛產品代工、肌膚保養產品代工、肌膚清潔產品代工、家庭清潔產品代工〉
本文由創馳生技法規顧問團隊編撰。我們結合多年的化妝品 OEM/ODM 實務經驗與衛福部最新規範,致力於協助品牌商在法規變動的時代中,穩健經營並合法上市。
※ 法規資料如有變動,仍須依照最新發布之公告規定辦理 ※
更新日期:2026/3/3
原文日期:2023/8/1

